太原理工大学|彭郅众,钟达忠,赵强,等:Ag-Sn间电子结构调控在酸性环境中实现1 A/cm2下高效CO2还原
Ag-Sn间电子结构调控在酸性环境中实现1 A/cm2下高效CO2还原
(太原理工大学化学与化工学院,气体能源高效清洁利用山西省重点实验室,山西 太原 030024)
DOI:10.11949/0438-1157.20250288
摘 要酸性条件下的电催化二氧化碳还原(CO2RR)因其能够提高CO2利用率并抑制碳酸盐形成而备受关注。然而,酸性环境由于H+浓度升高导致竞争性析氢反应(HER)加剧,从而对催化剂的稳定性和选择性提出了更高的要求。在此,报道了一种Ag-Sn双金属催化剂,在pH=2的酸性膜电极中表现出了优异的CO2RR性能。该催化剂在400 mA/cm2的电流密度下CO选择性高达99.4%,且在1 A/cm2的条件下,CO的法拉第效率(FECO)仍能维持在83.5%,CO的分电流密度最高达到了834.8 mA/cm2。研究发现,少量Sn的引入能够调节Ag的电子结构,从而加速CO2活化以及向*COOH中间体的转变。这项工作为开发适用于酸性条件的高效稳定CO2RR催化剂提供了新的思路。关键词酸性;电催化CO2还原;MEA;法拉第效率;CO分电流密度;电子结构;活化;中间体引用本文:彭郅众, 郎学磊, 房强, 井慧芳, 钟达忠, 李晋平, 赵强. Ag-Sn间电子结构调控在酸性环境中实现1 A/cm2下高效CO2还原[J]. 化工学报, 2025, 76(12): 6376-6386(PENG Zhizhong, LANG Xuelei, FANG Qiang, JING Huifang, ZHONG dazhong, LI Jinping, ZHAO Qiang. Ag-Sn interfacial electronic structure modulation for high-efficiency CO2 electroreduction at 1 A/cm2 under acidic conditions[J]. CIESC Journal, 2025, 76(12): 6376-6386)
引 言
随着全球碳排放问题日益严峻,二氧化碳的捕集和利用已成为当前的研究热点[1-2]。在众多二氧化碳还原反应中(电催化[3]、光催化[4]、热催化[5]、生物催化[6]),电催化二氧化碳还原反应(CO2RR)因其能够将CO2转化为高附加值燃料和化学品(如CO[7]、甲酸[8]、乙烯[9]、乙醇[10]等)而备受关注,其中CO是电催化CO2还原反应中最具经济可行性的产物之一[11]。然而,在传统碱性或中性电解液体系中,CO2气体容易与电解液中的OH-反应生成碳酸盐,生成的碳酸盐会沉积在电极表面,从而增加电极电阻,阻塞气体输送通道,并覆盖催化剂表面的活性位点;同时,碳酸根离子及碳酸氢根离子(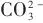 /
/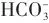 )在阳极电位的驱动下可以跨阴离子交换膜(AEM)迁移,并进一步与阳极产生的H+结合生成CO2。技术经济分析表明,阳极再生的CO2占能量输入的50%以上,这大大降低了能量效率(EE)[12-13]。因此,近中性和碱性电解质中的CO2RR通常稳定性和碳效率较低,这严重限制了其工业应用。近年来,酸性电解液体系中丰富的H+可以促进阴极CO2的再生[14],有效提高碳效率,同时电解槽中使用的质子交换膜(CEM)可以防止含碳的阴离子向阳极迁移,近年来成为一大研究热点。与此同时,CO2RR的实际应用受到反应物传质效率的严重制约。在传统H型电解槽中,通过溶解在水中的CO2参与反应,CO2在水中较低的溶解度[1 atm(1 atm=101.325 kPa)、25℃时仅为33 mmol/L]成了制约反应活性的主要因素,催化剂表面CO2传质速率不足,导致难以维持高电流密度下的持续反应[15]。流动电解槽相比H型电解槽有所改善,但仍受限于阴极电解液的离子传递速率,虽然能达到较高的电流密度,但能耗相对较大,并不能完全适用于工业体系。膜电极(MEA)组件(图1)中催化剂与离子交换膜直接接触,能以最低的能量损耗实现工业级电流密度,相较于H型电解槽和流动电解槽具有显著优势[16-17]。此外,MEA产物分离简单,易于模块化和规模化,适合工业化应用,尤其在可再生能源存储和绿色化学品合成领域前景广阔[18]。然而,酸性条件下高质子浓度引发剧烈的竞争性析氢反应(HER),以及高电流下的催化剂稳定性问题,使其在MEA体系中的大规模应用仍极具挑战[19-20]。图1MEA电解槽示意图Fig.1Schematic of MEA cell目前,一些金属催化剂,如碳包覆结构[21]以及分散的金属单原子[22]已被广泛应用于CO的生产。尽管CO法拉第效率能达到90%以上,但电流密度往往低于工业要求(200 mA/cm2)。银(Ag)基催化剂因其本身具有良好的CO选择性,常被用于碱性或中性CO2RR[23-24],这得益于其*CO中间体吸附较弱,容易解吸生成CO,但其在酸性介质中的活性位点易被H+覆盖,导致高电流密度下选择性急剧下降[25]。研究表明,通过引入亲氧金属调节Ag的电子结构,可优化*COOH中间体的吸附能并抑制HER副反应[26-27]。然而,酸性体系下第二金属掺杂引发电子结构的改变以及对中间体吸附的构效关系和作用机制仍需进一步验证。本文利用化学还原法精准合成了一系列不同比例的Ag-Sn双金属催化剂,并在酸性(pH=2)MEA体系中展现了优异的CO2RR性能。深入探究了Sn的掺入对Ag电子结构的影响,揭示了Ag表面电子结构变化对反应过程中关键中间体的影响规律。此外,还考察了催化剂制备过程中pH、催化剂负载量等关键因素对产物选择性的调控作用,以及Sn掺入量对活性位点暴露程度的影响,为后续的研究提供有利参考。氢氧化钠(NaOH,纯度96%),国药集团化学试剂有限公司;硝酸银[AgNO3,纯度99.8%],北京伊诺凯科技有限公司;硼氢化钠(NaBH4,纯度98.0%),上海阿拉丁生化科技股份有限公司;二水氯化亚锡(SnCl2·2H2O,纯度98%),国药集团化学试剂有限公司;实验用水是电阻率为18.25 MΩ·cm的去离子水。首先,将5 ml SnCl2·2H2O(0.05 mol/L)和5 ml Ag(NO)3(1 mol/L)依次加入80 ml去离子水中。随后,向混合溶液中加入7 ml NaOH(1 mol/L),充分搅拌使混合物均匀。最后,缓慢加入10 ml NaBH4(0.5 mol/L),以完成还原反应。反应结束后,通过离心分离产物,并在室温下进行真空干燥。为获得不同锡含量的样品,调整了SnCl2·2H2O的浓度:分别添加0.1 mol/L SnCl2·2H2O溶液和0.03 mol/L SnCl2·2H2O溶液,其余制备条件保持不变。最终产物中的Sn含量通过电感耦合等离子体(ICP)测定。采用相同方法制备了纯银纳米粒子(不添加SnCl2·2H2O)。为防止Ag+水解和NaBH4分解,所有溶液均需现配现用。催化剂油墨配制:精确称取40.5 mg催化剂粉末,与4 ml异丙醇及120 μl Nafion溶液[5%(质量分数)]混合,采用超声处理30 min,获得均匀分散的油墨。选取4.5 cm×4.5 cm疏水碳纸(YLS-30T)作为气体扩散层,使用喷枪将油墨均匀喷涂,最终控制催化剂总载量约为2 mg/cm2,随后将碳纸置于室温下干燥2 h,裁剪成1 cm×1 cm置于电解槽中进行测试。使用安捷伦气相色谱仪(HS-GC system)测试催化剂对各种气相产物的选择性;使用X射线衍射仪(XRD,Bruker D8 advance)分析催化剂的相组成;通过场发射扫描电子显微镜(SEM,JEOL JEM 2100F)对催化剂的表面形貌进行表征;利用扫描电子显微镜(SEM,HITACHI SU8000)和透射电子显微镜(TEM,JEOL JEM-2100F)对催化剂的形貌及表面元素分布进行表征;通过X射线光电子能谱仪(XPS,Thermo Scientific K-alpha)测定催化剂的金属价态(XPS数据在使用前均与C的标准峰284.8 eV进行了校正);采用电感耦合等离子体发射光谱(ICP-OES,Optima 8300)对催化剂中Ag和Sn的比例进行定量分析。使用膜电极组件(MEA)测试催化剂在酸性CO2RR过程中的性能。MEA电解槽是两电极体系,可以有效避免CO2溶解度低的问题,从而提高电流密度。阴极室和阳极室通过质子交换膜(Nafion 117)隔开,阳极催化剂为负载在钛网上的IrO2。测试通过电化学工作站(PARSTAT PMC-1000)施加反应所需的电流,CO2气体通过润湿进入阴极,使用气体流量计将CO2的流量控制在50 cm3/min(标准工况)。阳极产生的气体通过气液混合泵从阳极中排出。阴极出口连接有热导检测器(TCD)的气相色谱仪(Agilent 8890),用于分析产物成分。根据施加电流及气相色谱测定的气体浓度计算法拉第效率。通过化学还原法制备了不同比例的银/锡纳米颗粒及银纳米颗粒(Ag NP),利用过量的硼氢化钠使反应还原充分,制备过程见图2。通过控制Ag、Sn投料获得不同比例的样品,根据ICP测定实际的银锡含量,分别命名为Ag-Sn4.9%、Ag-Sn1.4%、Ag-Sn0.2%。图2Ag-Sn1.4%的制备流程图Fig.2The scheme for the preparation of Ag-Sn1.4%利用X射线衍射仪对Ag-Sn催化剂结构进行表征。XRD谱图在38.1°、44.3°、64.4°、77.5°和81.5°处出现的衍射峰分别对应于Ag的(111)、(200)、(220)、(311)和(222)晶面[图3(a)]。XRD谱图中未出现Sn的特征峰,可能是其掺杂较少导致被覆盖或稀释在Ag的晶格中[27]。同时,观察到随着Sn掺杂量的增加,衍射峰的强度逐渐减弱,这表明Sn掺杂在一定程度上影响了Ag的晶体结构[28]。用X射线光电子能谱仪(XPS)测定了银/锡的化学组成和价态,结果如图3(b)~(d)所示。由图可知,不同比例的Ag-Sn催化剂的Ag 3d光谱和Sn 3d光谱对应的特征峰分别对应于Ag和Sn的零价金属态,证明了Sn成功掺入。图3(a) Ag-Sn及Ag NP的XRD谱图;(b~d) Ag-Sn4.9%,Ag-Sn1.4%,Ag-Sn0.2%的XPS谱图Fig.3(a) XRD of Ag-Sn and Ag NP; XPS for (b) Ag-Sn4.9%; (c) Ag-Sn1.4%; (d) Ag-Sn0.2%使用扫描电子显微镜分析了不同Sn含量的Ag-Sn催化剂及Ag NP的表面形貌。如图4(a)~(d)所示,Ag-Sn催化剂和Ag NP具有相同的纳米形态。随着Sn掺杂量的增加,颗粒尺寸减小,并趋向于较为聚集的形态,这与XRD衍射峰强度变化结果相一致。透射电子显微镜图[图5(a)~(d)]显示Ag-Sn1.4%和Ag NP晶格间距为2.46 Å(1Å=0.1 nm)和2.38 Å,与银的(111)晶面接近,这与XRD对应的Ag的标准卡片结果相一致。Ag(111)晶面是原子排列最紧密的晶面,表面能较低且热力学稳定[29],有利于CO2分子以及含碳中间体的吸附与活化,使反应朝向既定的路径进行。能谱图[图6(a)~(d)]证实了Ag-Sn1.4%中Ag和Sn的存在,且Sn在其中均匀分布。图4(a)Ag NP、(b)Ag-Sn0.2%、(c)Ag-Sn1.4%、(d)Ag-Sn4.9%的扫描电镜图Fig.4SEM of (a) Ag NP, (b) Ag-Sn0.2%, (c) Ag-Sn1.4%, (d) Ag-Sn4.9%图5(a)Ag-Sn1.4%的透射电镜图;(b)Ag-Sn1.4%的高分辨率透射电镜图;(c)Ag NP的透射电镜图;(d)Ag NP的高分辨率透射电镜图Fig.5(a) TEM of Ag-Sn1.4%; (b) HRTEM of Ag-Sn1.4%; (c) TEM of Ag NP; (d) HRTEM of Ag NP图6Ag-Sn1.4%的mapping图Fig.6Mapping of Ag-Sn1.4%本工作通过微量Sn掺杂成功调控了Ag的电子结构,优化了Ag表面CO2活化及*COOH的生成过程,最大的程度地抑制了析氢反应,提高CO2RR效率,使其在400 mA/cm2的电流密度下CO选择性高达99.4%,且1 A/cm2的条件下,CO的法拉第效率仍能维持在83.5%,CO的分电流密度最高达到了834.8 mA/cm2。这一突破为开发适用于酸性环境的高效CO2电还原催化剂提供了理论依据。未来需进一步探究催化剂的长期稳定性以推动CO2电解技术的实际应用进程。
)在阳极电位的驱动下可以跨阴离子交换膜(AEM)迁移,并进一步与阳极产生的H+结合生成CO2。技术经济分析表明,阳极再生的CO2占能量输入的50%以上,这大大降低了能量效率(EE)[12-13]。因此,近中性和碱性电解质中的CO2RR通常稳定性和碳效率较低,这严重限制了其工业应用。近年来,酸性电解液体系中丰富的H+可以促进阴极CO2的再生[14],有效提高碳效率,同时电解槽中使用的质子交换膜(CEM)可以防止含碳的阴离子向阳极迁移,近年来成为一大研究热点。与此同时,CO2RR的实际应用受到反应物传质效率的严重制约。在传统H型电解槽中,通过溶解在水中的CO2参与反应,CO2在水中较低的溶解度[1 atm(1 atm=101.325 kPa)、25℃时仅为33 mmol/L]成了制约反应活性的主要因素,催化剂表面CO2传质速率不足,导致难以维持高电流密度下的持续反应[15]。流动电解槽相比H型电解槽有所改善,但仍受限于阴极电解液的离子传递速率,虽然能达到较高的电流密度,但能耗相对较大,并不能完全适用于工业体系。膜电极(MEA)组件(图1)中催化剂与离子交换膜直接接触,能以最低的能量损耗实现工业级电流密度,相较于H型电解槽和流动电解槽具有显著优势[16-17]。此外,MEA产物分离简单,易于模块化和规模化,适合工业化应用,尤其在可再生能源存储和绿色化学品合成领域前景广阔[18]。然而,酸性条件下高质子浓度引发剧烈的竞争性析氢反应(HER),以及高电流下的催化剂稳定性问题,使其在MEA体系中的大规模应用仍极具挑战[19-20]。图1MEA电解槽示意图Fig.1Schematic of MEA cell目前,一些金属催化剂,如碳包覆结构[21]以及分散的金属单原子[22]已被广泛应用于CO的生产。尽管CO法拉第效率能达到90%以上,但电流密度往往低于工业要求(200 mA/cm2)。银(Ag)基催化剂因其本身具有良好的CO选择性,常被用于碱性或中性CO2RR[23-24],这得益于其*CO中间体吸附较弱,容易解吸生成CO,但其在酸性介质中的活性位点易被H+覆盖,导致高电流密度下选择性急剧下降[25]。研究表明,通过引入亲氧金属调节Ag的电子结构,可优化*COOH中间体的吸附能并抑制HER副反应[26-27]。然而,酸性体系下第二金属掺杂引发电子结构的改变以及对中间体吸附的构效关系和作用机制仍需进一步验证。本文利用化学还原法精准合成了一系列不同比例的Ag-Sn双金属催化剂,并在酸性(pH=2)MEA体系中展现了优异的CO2RR性能。深入探究了Sn的掺入对Ag电子结构的影响,揭示了Ag表面电子结构变化对反应过程中关键中间体的影响规律。此外,还考察了催化剂制备过程中pH、催化剂负载量等关键因素对产物选择性的调控作用,以及Sn掺入量对活性位点暴露程度的影响,为后续的研究提供有利参考。氢氧化钠(NaOH,纯度96%),国药集团化学试剂有限公司;硝酸银[AgNO3,纯度99.8%],北京伊诺凯科技有限公司;硼氢化钠(NaBH4,纯度98.0%),上海阿拉丁生化科技股份有限公司;二水氯化亚锡(SnCl2·2H2O,纯度98%),国药集团化学试剂有限公司;实验用水是电阻率为18.25 MΩ·cm的去离子水。首先,将5 ml SnCl2·2H2O(0.05 mol/L)和5 ml Ag(NO)3(1 mol/L)依次加入80 ml去离子水中。随后,向混合溶液中加入7 ml NaOH(1 mol/L),充分搅拌使混合物均匀。最后,缓慢加入10 ml NaBH4(0.5 mol/L),以完成还原反应。反应结束后,通过离心分离产物,并在室温下进行真空干燥。为获得不同锡含量的样品,调整了SnCl2·2H2O的浓度:分别添加0.1 mol/L SnCl2·2H2O溶液和0.03 mol/L SnCl2·2H2O溶液,其余制备条件保持不变。最终产物中的Sn含量通过电感耦合等离子体(ICP)测定。采用相同方法制备了纯银纳米粒子(不添加SnCl2·2H2O)。为防止Ag+水解和NaBH4分解,所有溶液均需现配现用。催化剂油墨配制:精确称取40.5 mg催化剂粉末,与4 ml异丙醇及120 μl Nafion溶液[5%(质量分数)]混合,采用超声处理30 min,获得均匀分散的油墨。选取4.5 cm×4.5 cm疏水碳纸(YLS-30T)作为气体扩散层,使用喷枪将油墨均匀喷涂,最终控制催化剂总载量约为2 mg/cm2,随后将碳纸置于室温下干燥2 h,裁剪成1 cm×1 cm置于电解槽中进行测试。使用安捷伦气相色谱仪(HS-GC system)测试催化剂对各种气相产物的选择性;使用X射线衍射仪(XRD,Bruker D8 advance)分析催化剂的相组成;通过场发射扫描电子显微镜(SEM,JEOL JEM 2100F)对催化剂的表面形貌进行表征;利用扫描电子显微镜(SEM,HITACHI SU8000)和透射电子显微镜(TEM,JEOL JEM-2100F)对催化剂的形貌及表面元素分布进行表征;通过X射线光电子能谱仪(XPS,Thermo Scientific K-alpha)测定催化剂的金属价态(XPS数据在使用前均与C的标准峰284.8 eV进行了校正);采用电感耦合等离子体发射光谱(ICP-OES,Optima 8300)对催化剂中Ag和Sn的比例进行定量分析。使用膜电极组件(MEA)测试催化剂在酸性CO2RR过程中的性能。MEA电解槽是两电极体系,可以有效避免CO2溶解度低的问题,从而提高电流密度。阴极室和阳极室通过质子交换膜(Nafion 117)隔开,阳极催化剂为负载在钛网上的IrO2。测试通过电化学工作站(PARSTAT PMC-1000)施加反应所需的电流,CO2气体通过润湿进入阴极,使用气体流量计将CO2的流量控制在50 cm3/min(标准工况)。阳极产生的气体通过气液混合泵从阳极中排出。阴极出口连接有热导检测器(TCD)的气相色谱仪(Agilent 8890),用于分析产物成分。根据施加电流及气相色谱测定的气体浓度计算法拉第效率。通过化学还原法制备了不同比例的银/锡纳米颗粒及银纳米颗粒(Ag NP),利用过量的硼氢化钠使反应还原充分,制备过程见图2。通过控制Ag、Sn投料获得不同比例的样品,根据ICP测定实际的银锡含量,分别命名为Ag-Sn4.9%、Ag-Sn1.4%、Ag-Sn0.2%。图2Ag-Sn1.4%的制备流程图Fig.2The scheme for the preparation of Ag-Sn1.4%利用X射线衍射仪对Ag-Sn催化剂结构进行表征。XRD谱图在38.1°、44.3°、64.4°、77.5°和81.5°处出现的衍射峰分别对应于Ag的(111)、(200)、(220)、(311)和(222)晶面[图3(a)]。XRD谱图中未出现Sn的特征峰,可能是其掺杂较少导致被覆盖或稀释在Ag的晶格中[27]。同时,观察到随着Sn掺杂量的增加,衍射峰的强度逐渐减弱,这表明Sn掺杂在一定程度上影响了Ag的晶体结构[28]。用X射线光电子能谱仪(XPS)测定了银/锡的化学组成和价态,结果如图3(b)~(d)所示。由图可知,不同比例的Ag-Sn催化剂的Ag 3d光谱和Sn 3d光谱对应的特征峰分别对应于Ag和Sn的零价金属态,证明了Sn成功掺入。图3(a) Ag-Sn及Ag NP的XRD谱图;(b~d) Ag-Sn4.9%,Ag-Sn1.4%,Ag-Sn0.2%的XPS谱图Fig.3(a) XRD of Ag-Sn and Ag NP; XPS for (b) Ag-Sn4.9%; (c) Ag-Sn1.4%; (d) Ag-Sn0.2%使用扫描电子显微镜分析了不同Sn含量的Ag-Sn催化剂及Ag NP的表面形貌。如图4(a)~(d)所示,Ag-Sn催化剂和Ag NP具有相同的纳米形态。随着Sn掺杂量的增加,颗粒尺寸减小,并趋向于较为聚集的形态,这与XRD衍射峰强度变化结果相一致。透射电子显微镜图[图5(a)~(d)]显示Ag-Sn1.4%和Ag NP晶格间距为2.46 Å(1Å=0.1 nm)和2.38 Å,与银的(111)晶面接近,这与XRD对应的Ag的标准卡片结果相一致。Ag(111)晶面是原子排列最紧密的晶面,表面能较低且热力学稳定[29],有利于CO2分子以及含碳中间体的吸附与活化,使反应朝向既定的路径进行。能谱图[图6(a)~(d)]证实了Ag-Sn1.4%中Ag和Sn的存在,且Sn在其中均匀分布。图4(a)Ag NP、(b)Ag-Sn0.2%、(c)Ag-Sn1.4%、(d)Ag-Sn4.9%的扫描电镜图Fig.4SEM of (a) Ag NP, (b) Ag-Sn0.2%, (c) Ag-Sn1.4%, (d) Ag-Sn4.9%图5(a)Ag-Sn1.4%的透射电镜图;(b)Ag-Sn1.4%的高分辨率透射电镜图;(c)Ag NP的透射电镜图;(d)Ag NP的高分辨率透射电镜图Fig.5(a) TEM of Ag-Sn1.4%; (b) HRTEM of Ag-Sn1.4%; (c) TEM of Ag NP; (d) HRTEM of Ag NP图6Ag-Sn1.4%的mapping图Fig.6Mapping of Ag-Sn1.4%本工作通过微量Sn掺杂成功调控了Ag的电子结构,优化了Ag表面CO2活化及*COOH的生成过程,最大的程度地抑制了析氢反应,提高CO2RR效率,使其在400 mA/cm2的电流密度下CO选择性高达99.4%,且1 A/cm2的条件下,CO的法拉第效率仍能维持在83.5%,CO的分电流密度最高达到了834.8 mA/cm2。这一突破为开发适用于酸性环境的高效CO2电还原催化剂提供了理论依据。未来需进一步探究催化剂的长期稳定性以推动CO2电解技术的实际应用进程。Ag-Sn interfacial electronic structure modulation for high-efficiency CO2 electroreduction at 1 A/cm2 under acidic conditions
PENG Zhizhong LANG XueleiFANG QiangJING HuifangZHONG dazhongLI JinpingZHAO Qiang
LANG XueleiFANG QiangJING HuifangZHONG dazhongLI JinpingZHAO Qiang
(Shanxi Key Laboratory of Gas Energy Efficient and Clean Utilization, College of Chemistry and Chemical Engineering, Taiyuan University of Technology, Taiyuan 030024, Shanxi, China)
Abstract: Electrocatalytic CO2 reduction under acidic conditions has attracted significant attention due to its ability to enhance CO2 utilization and suppress carbonate formation. However, the elevated H+ concentration in acidic environments intensifies the competing hydrogen evolution reaction (HER), thereby imposing higher requirements on catalyst stability and selectivity. Herein, we report an Ag-Sn bimetallic catalyst that exhibits outstanding CO2RR performance in an acidic membrane electrode assembly (MEA) at pH=2. Under a current density of 400 mA/cm2, the catalyst achieves a CO selectivity of up to 99.4%, and even at 1 A/cm2, the CO Faraday efficiency (FECO) remains at 83.5%, with a maximum CO partial current density reaching 834.8 mA/cm2. The study found that the introduction of a small amount of Sn can adjust the electronic structure of Ag, thereby accelerating the activation of CO2 and the transformation to *COOH intermediates. This work provides a new strategy for developing highly efficient and stable CO2RR catalysts suitable for operation under acidic conditions.Keywords: acid;electrocatalytic carbon dioxide reduction;MEA;Faraday efficiency;CO partial current density;electronic structure;activation;intermediate第一作者:彭郅众(1998—),男,硕士研究生,pengzhizhong1054@link.tyut.edu.cn
通讯作者:钟达忠(1992—),男,博士,助理研究员,zhongdazhong@tyut.edu.cn;赵强(1978—),男,博士,教授,zhaoqiang@tyut.edu.cn